图像作为学科重点和考试重点
现代化学是科学革命的结果,更是乘着20世纪量子力学的发展高歌猛进,成为现代科学的重点学科。AP化学开篇就从原子的微观结构讲起,相比于自然哲学时代的“眼见为实”,现代化学建立在高精密的科学仪器和数据基础上。因此分析仪器谱图是化学人必备素质。
但是同学们毕竟没用亲自用过现代仪器,往往是通过老师在白板上绘画原理,举例说明。毕竟不够直观,因此对相当多同学而言,仪器谱图分析是老大难问题。
TD AP化学明星教师——杨行老师通过本篇文章总结梳理了AP考试必考的谱图题,希望同学们通过总结对比掌握看图的一般方法和解决常见问题的套路。

AP当中的7类常见图像
1.质谱 Mass spectrometer
质谱是Unit 1知识点,该图像最重要的信息是同一原子的不同同位素(isotope)可以考察其含量。横坐标一般是相对原子质量(amu),也可以是m/z(一般默认电荷量z为1)。纵坐标为该种同位素丰度(abundance)。
具体考法,根据横坐标相对原子质量*纵坐标的百分含量加和求加权平均数后可得该种原子的平均相对分子质量,也就是周期表中的数据。从而分辨原子,分析同位素的信息。
如下图2015-03,可以该物质平均分子量介于90-92之间。

2.光电子能谱 PES, photoelectron spectrum
光电子能谱也是Unit 1的知识点,该图像能够反应核外电子按照能级(sublevel)进行排列的情况。该图谱横坐标为结合能binding energy,纵坐标为电子数目。最大的陷阱在于横坐标轴是左大右小。因此从左往右可以依次判断为1s、2s、2p、3s……,纵坐标是该能级上的电子数目。如下图2019年第19题。左侧为3电子Li,右侧为斯电子Be。
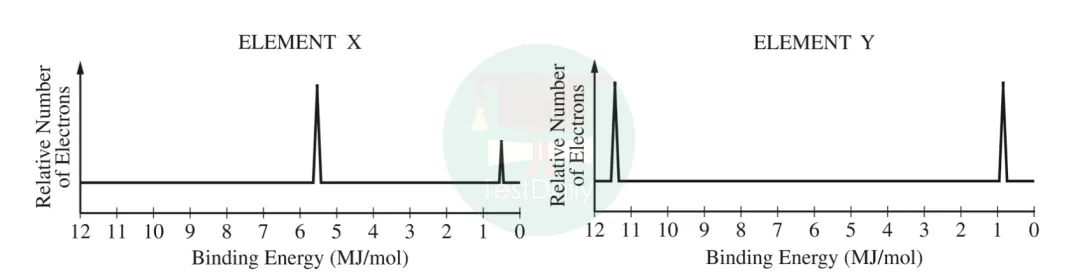
2016年第35题,属于只判断1s电子的binding energy,只由质子总数决定。

3.路易斯结构式 Lewis diagram
路易斯结构式在Unit 2中学习,可广泛用于各章知识考察。用点/叉表示电子,用直线表示共价键,以此表明一个分子或者离子团的组成。请注意,图像中画出的平面结构不是真实结构。
经常结合的考点是分子构型的判断,键角、杂化判断。基于分子结构的分之间作用力判断。比如2019年42题,最左侧的N有四根单键,应该形成tetrahedral构型,键角109.5°,sp2杂化。

再比如2017年20题,左侧化合物一的N没有连接H,因此左右的化合物一不能形成氢键,而右侧的化合物二可以形成氢键。

4.麦克斯韦-玻尔兹曼分布 Maxwell-Boltzmann distribution
这个分布会在Unit 3中学习气体动理论(KMT)时学习,也经常用于解释Unit 5中温度和催化剂如何影响反应速率的的问题。横坐标是分子运动的速度/动能,纵坐标是不同速度/动能对应的数目。因此温度越高,分子平均动能越大,曲线右移,跨度变大会变得更矮。
如2018第27题,B是代表更高温度的情况,而不是像同学们一般推测的更高的曲线代表更高温的气体,运动速度在横坐标。

5.浓度-时间曲线
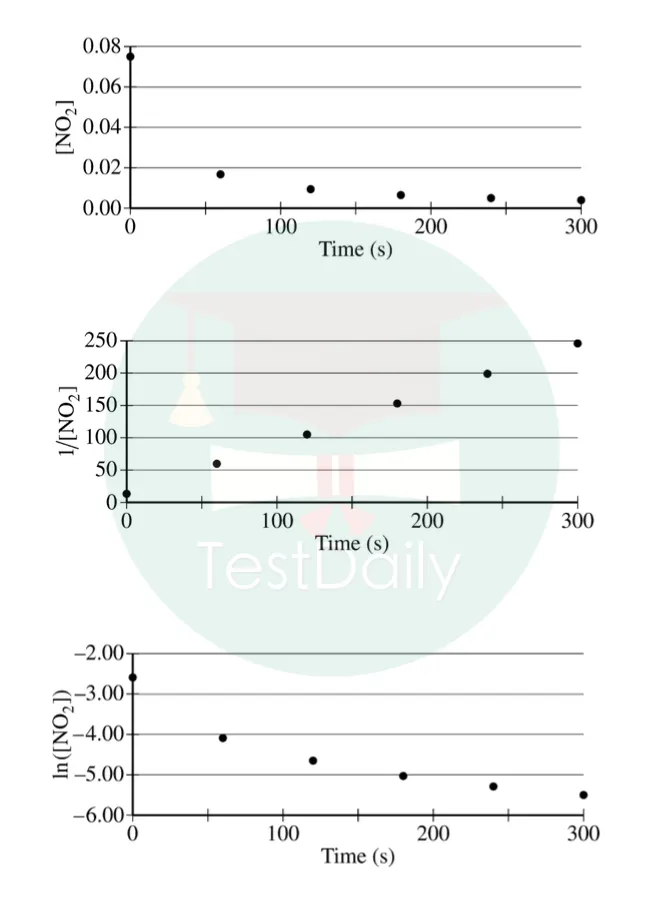
Unit 5中结合公示表的三种反应级数对应的反应,以及速率积分函数的表达式进行的分析。如下图公式表中所给出的,浓度对时间线性关系(0级反应),ln[反应物]对时间线性关系(1级反应);1/[反应物]对时间线性关系(2级反应)。

比如2019-FRQ第6题可知第二个1/[反应物]对时间线性关系,这是一个二级反应。
6.分光光度计 Spectrophotometer,吸光度图像 Absorbance
Unit 3第一次学习,基本原理是光通过溶液会被吸收,吸收程度同溶液浓度成正比,也可以表达为beer’s law, A=abc。横坐标是溶液浓度,纵坐标是吸光度。
如2022-FRQ第6(b)题,浓度越大,吸光值越大。
考试有两种考法,根据吸光度计算未知组分浓度;或分析异常数据原因。
例如下面这张图中,异常数据点在拟合线下方,即实际吸光度比预期偏低,通常是因为溶液的实际浓度比预期浓度偏低,进而可分析造成浓度偏低的原因。

7.pH曲线
学习于Unit 8,常常配合酸碱滴定实验考察。横坐标是滴定剂(titrant)的用量,随着反应不断进行。纵坐标pH发生变化。图像中一共有四个需要注意的点。A起始点,强酸的pH可以根据浓度直接计算;弱酸的pH要更大。B滴定终点,强酸强碱混合pH=7,弱酸强碱混合pH>7强酸弱碱混合pH<7。C半滴定终点,存在弱酸或者弱碱,pH=pKa。D 无限远点,pH趋近于所用滴定剂的pH。
比如2022-FRQ 第1(d)题,通过滴定终点pH>7可知这是弱酸中加入强碱;根据半滴定终点可知该酸的pKa=3.1.

图像分析的一般方法
1️⃣重点关注横纵坐标,PES, maxwell-boltzmann distribution都是容易误看横坐标的图像。
2️⃣曲线表达趋势性往往来源于某一公式,比如吸光度正比于浓度
3️⃣曲线不要盯着线看,关注重要的节点,比如pH曲线上的equivalence point,half equivalence point。
4️⃣示意图往往不代表真实物质,但体现关键信息,比如lewis diagram。
本文作者

TD福利&领取方式
TD为大家准备了适合在考前对知识点进行查缺补漏的神器——「AP化学考点精华」,扫描下方二维码添加马甲并回复暗号「化学考点」即可领取~


(AP化学考点精华封面预览)








