AP化学酸碱与粒子观
酸和碱(Acid and base)是AP化学考试大纲中Unit 8的内容,考试占比11%-15%,是全部九个章节当中占比第二高的章节,仅次于Unit 3。
酸碱章节也是考试难度最大的章节,在2022年考试中0分率最高的章节就是本章节。
在我们对学员进行学术摸底和模考测评当中,无论是实际得分还是同学们的心态反馈,都把酸碱当做“头号敌人”;考虑到酸碱的特别难度,TD每年的AP化学教学都格外的侧重本章节,无论是课时分配还是练习册的题量安排都有很大的倾斜,这样的举措在过去为历年的TD化学学员赢得了更多的5分机会;但我们相信仍然有很多学员宥于该“酸碱天堑”。
溶液世界的粒子类型
理解酸碱溶液中的种种变化,要能透过化学符号看到其背后的存在的到底是什么粒子。而能够有效区分离子(ions, including cations and anions)、分子(molecules)是需要从Unit 2、4就妥善训练的正确的粒子和作用力观念。这当中又叠加了物质的固体到溶液态的转化,就需要分类讨论清楚。
1.溶液中的离子ions in aqueous solution
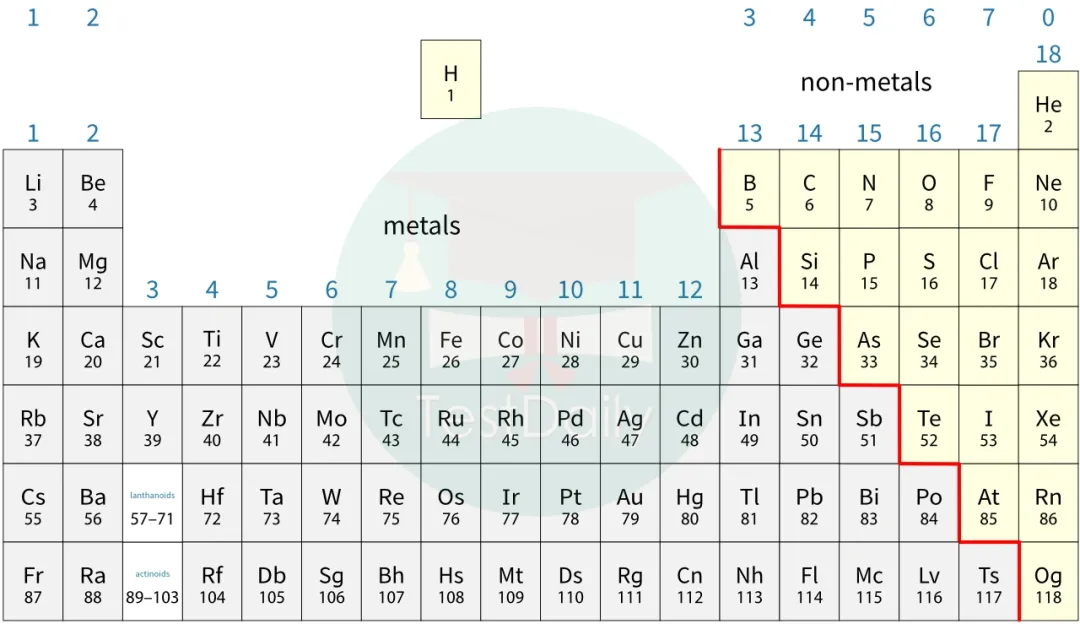
一般来讲,金属与非金属之间形成ionic bond。其内在逻辑的简化版是金属元素在周期表中占据左下角,原子半径比较大,原子核与最外层电子距离较远,易失电子形成阳离子(cation)。非金属元素在周期表中占据周期表右上角,原子半径比较小,原子核与最外层电子距离比较近,容易吸引电子形成阴离子(anion)。
在固体形态时,是通过阴阳离子正负电荷之间的吸引力交错堆积形成固体,以最常见的NaCl为例如下图所示,在这层面上已经没有原子(atoms)了,只有作为阳离子的Na+,和作为阴离子的Cl-。

当它溶于水成为溶液状态时,阴阳离子分别独立存在,如下图所示;这一点至关重要。很多同学会认为存在一个溶液态的NaCl的整体,这是错误的。

因此其反应的粒子行为也是独立的,完全可以Cl-与其他另一种阳离子比如Ag+形成沉淀,而Na+在旁观。
挑战是同学们习惯了用化学方程式写出其变化,因此学习从化学方程式到离子方程式的转化是弄清楚粒子层面真实变化的必要前置。如果这里有问题建议同学们先复习好Unit 4当中的ionic equation部分。

2.溶液中的分子molecules in aqueous solution
分子(molecules)是有原子通过共价键(covalent bond)形成的,分子是在物理或者化学变化层面独立发生变化的单元。比如水分子。分子在其固液气状态时都是单独存在的一级粒子,麻烦发生在溶液状态。
强酸比如HCl,在水溶液中因为电离成为独立存在的两种粒子H+,Cl-,更重要的是弱酸分子的小部分电离性质使得弱酸溶液当中弱酸主要以分子形式存在,而不是带正负电的离子存在。如下图。

3.离子和分子在酸碱反应中的体现ions & molecules in acid and base reaction

强酸强碱在溶液中以ions的形式存在,它的反应对于阴阳离子部分是完全独立存在的;
而弱酸在溶液中大多数以molecules的形式存在,因此,同样和碱反应。氢氧根消耗掉强酸的氢离子,是单独的离子行为。对于弱酸是结合弱酸分子当中的H+部分从生成水从而生成了弱酸的共轭碱离子(ions of conjugate base)。
因此其ionic equation如下图所示。

AP化学考法
正确的酸碱粒子观是正确理解酸碱和反应的前提,本身也作为一个直接的知识点来进行考察。比如2023 FRQ-5(C),如下图。

图中同时存在作为分子的HA和HA的电离产物,两种阴阳离子H+,A-。因此可知这是一种不完全电离的酸,属于弱酸。
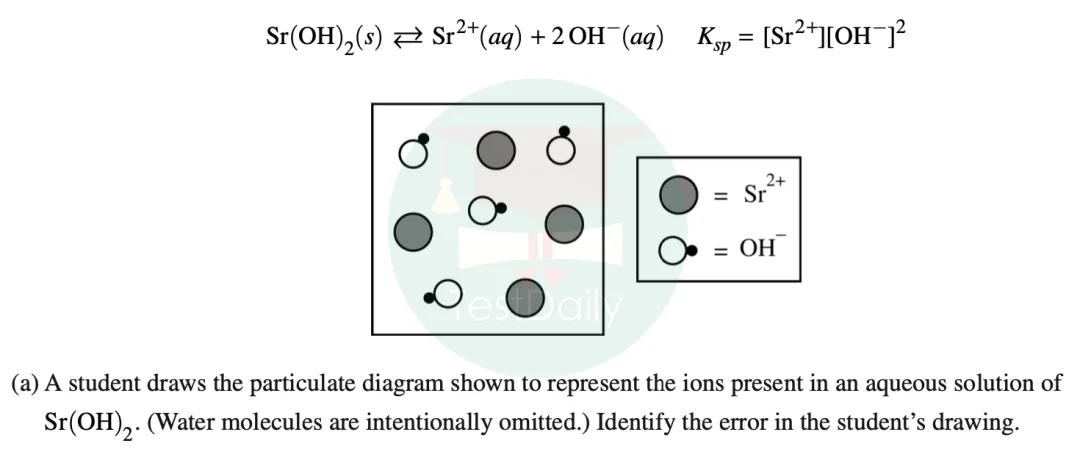
而建立在这种粒子观基础上的,也帮助其他章节比如Unit 7中solubility equilibrium。诸如2023 FRQ-7(a)。这里没有作为一个整体存在的Sr(OH)2,只有已经电离了的阴阳离子。
结语
有了正确的粒子观不仅能直接解决对应的粒子图像问题,根据粒子图像推算各种物质的比例;更进而给予粒子写出可能存在的ionic equation;利用ionic equation分析pH的变化,或者构造出来的buffer的pH,或者titration的计算等。
以上就是基于正确粒子观的三层次acid and base考察。
本文作者
TD福利&领取方式
TD为大家准备了适合在考前对知识点进行查缺补漏的神器——「AP化学考点精华」,扫描下方二维码添加马甲并回复暗号「化学考点」即可领取~


(AP化学考点精华封面预览)










