
暑假的脚步越来越近,放松休息之余,申请er们又开始奔波在各大竞赛中。暑假期间是大家准备理科类竞赛的最佳时机,对于想要申请化学生物相关专业的同学而言,UKChO英国化学奥林匹克竞赛则是大家的不二之选。
在之前的推文中,TD 理科竞赛教师——杨行老师,针对UKChO竞赛中的重难点考察知识,给大家带来了《UKChO有机机理不会?从亲核取代反应带你学第一篇:SN2反应!》,今天则是本系列的第二篇分享,快跟小编一起来看看吧~

(一)复习亲核取代反应,从SN2到SN1
本系列文第一篇已经讲解了亲核取代反应的一般原理,并详细讲解了SN2反应的基本原理。我们在本文复习一下亲核取代反应的一般原理并重点学习SN1反应
1.亲核取代一般原理
亲核取代(Nucleophilic substitution,SN)是有机反应当中最基础最重要的反应机理类型之一。也是UKChO考试中有机题目一定会涉及的机理。其中电子密度高的物质称为亲核试剂,取代另一个缺电子分子(称为亲电子试剂)内的官能团。最一般的反应形式如下:

来自亲核试剂的电子对攻击底物R−LG并与其结合。同时,离去集团LG带着电子对离开。本例中的主要产物是R−Nuc。亲核试剂可以是电中性的或带负电的,而底物通常是中性的或带正电的。
2.SN2和SN1反应
tertiary三级碳倾向于发生SN1反应,越靠近primary一级碳就越倾向于发生SN2反应。那为什么会出现这种区别呢,这两种不同又是怎么表现出来的呢?请看下文
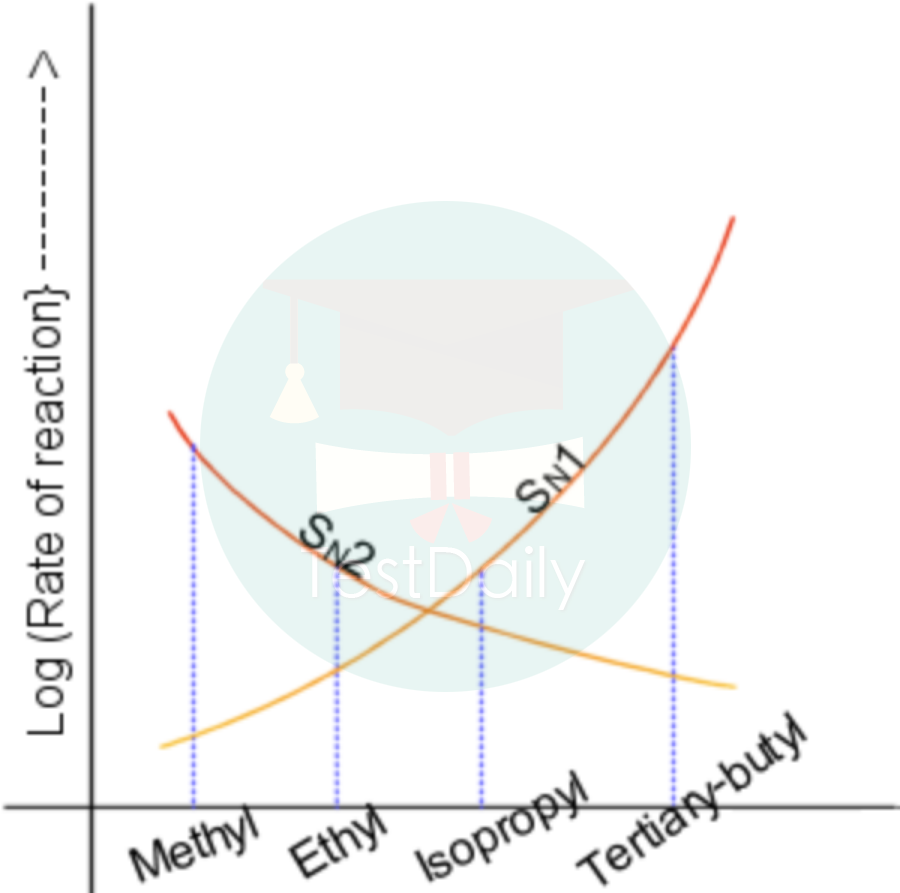
(二)单分子亲核取代反应SN1
1.单分子亲核取代SN1机理

单分子亲核取代SN1反应中S代表substitution取代反应,N代表nucleophilic亲核机理,1表示限速步骤(通常是第一步)是单分子的,也就是只有底物浓度影响反应速率,也称之为一级反应。
与SN2机制不同,该反应不太依赖于亲核试剂的强度,速率也不依赖亲核试剂的浓度,只取决于底料浓度。这是因为在SN1机理的第一步中,形成平面碳正离子是慢速步骤,也就是速率决定步骤。
最终会形成外消旋混合物,其原因就在于第一步离去集团自行离去形成了碳正离子,而碳正离子是平面构型。后续亲核试剂在进攻的时候也就不同于SN2反应的背侧进攻,而是从平面的两侧均等概率进攻。
2.神奇的碳正离子carbocation(进阶学员选读)
碳正离子示意图如下:
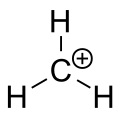
碳正离子是任何含有偶数电子的阳离子,其中大部分正电荷位于碳原子上。碳正离子的定义无论是历史还是现实都是一个难缠的问题,所以聪明的学员仅需要从图像的角度来把握即可,也就是中心碳原子表现sp2杂化如下图。

起码我们可以这样解释,一个带有正电荷的碳原子,该碳原子被六个价电子包围,而不是填充碳价层所需的通常八电子。因此,碳正离子通常具有反应性,因为它电子不够,它就试图填满把电子并重新获得电中性。根据VSEPR规则,三配位碳正离子通常是平面三角型,具有纯p特征空轨道作为其最低未占据分子轨道(LUMO)并且C-H/C-C键由sp2轨道形成。

邻近烷基的超共轭作用稳定了叔丁基阳离子。稳定相互作用可以描述为轨道相互作用或通过涉及“无键”共振形式的共振结构。(为了清楚起见,用虚线表示氢原子仍然附着,尽管超共轭结构中的形式C-H键级为零)
叔(三级)、仲(二级)和伯(一级)烷基碳鎓离子以及甲基阳离子(最右侧)示例的稳定性顺序如下。总结,三级碳正离子最稳定(烷烃基是给电子集团或者朝共轭作用)。

3.SN1反应实例
如下,一个三级溴代物反生水解生成三级醇。

?该反应分为三步进行:
从碳原子上离去溴阴离子,从而形成叔丁基碳正离子。该步骤很慢。注意,不同于SN2反应,该步骤的发生不需要亲核试剂的进攻。

亲核进攻:碳正离子与亲核试剂发生反应。如果亲核试剂是中性分子,进攻后亲核试剂相当于失电子带正电,则需要第三步来脱去质子。

碳正离子与亲核试剂重组如下图

去质子化:通过水作为碱去除质子化亲核试剂上的质子,形成醇和水合氢离子。这反应步骤很快。

4.SN1反应中的立体化学(进阶学员选读)
在反应速率决定步骤(第一步慢速步骤)中形成的碳正离子中间体是具有平面三角形分子几何形状的sp2杂化碳正离子。一个平面被进攻时,亲核试剂可以从两侧进攻而来。这就产生两种可能。如果被进攻的位置连接后是手性中心,则产生对映体的外消旋混合物(racemic mixture)。
比如,在S-3-氯-3-甲基己烷与碘离子的SN1反应中,第二步碘离子可以从碳正离子中间体的双侧进攻而来,从而产生S和R一比一的手性混合物,由于两侧进攻的概率是一致的,产物比例也是一比一,最后的混合物反而没有旋光性,多么神奇!

(三)SN2和SN1反应对比
SN1反应主要是发生在三级碳,SN2反应发生在一级碳;
SN1反应速率只有底物浓度决定,与亲核试剂浓度无关;SN2反应速率同时受底物和亲核试剂浓度影响;
SN1反应产物生成没有旋光性的外消旋物(如果有手性中心);SN2反应产物相较于底物构型翻转;
SN1反应的启动不依赖于亲核试剂的进攻;SN2反应的启动依赖于亲核试剂;
因此亲核试剂的性质和底物的空间位阻对SN2反应影响更大。
非常感谢杨行老师干货满满的分享,我们将在后续文章中持续为大家带来UKChO的教研文章,感兴趣的同学可以关注公众号持续观看哦~
本文作者

福利时刻
为帮助同学们快速了解UKChO比赛,TD整理了UKChO近年考试真题,免费分享给大家!扫下方二维码添加小马甲,发送暗号「UKChO」即可领取。
TD也有开设【UKChO备赛计划】,感兴趣的小伙伴也可以扫码了解更多哦!








